Catabasis: Alles zu gut, um wahr zu sein?
Catabasis Pharmaceuticals (WKN: A2PBC0) präsentiert aktuell auf dem größten Duchenne-Fachkongress der Welt, der Parent Project Muscular Dystrophy 25th Annual Conference in Orlando. Mit dabei ist die Crème de la Crème der in diesem lukrativen Sektor tätigen Pharmaelite. Das weckt Phantasie.
Im Rahmen erster Poster-Präsentationen veröffentlichte Catabasis gestern ein Update zum laufenden Enrollment seiner finalen Phase-3-Zulassungsstudie für Edasalonexent. Das Präparat hat das Potenzial zur neuen Grundtherapie für alle an der tödlichen Duchenne-Erkrankung leidenden Jungen zu werden. Darauf deuten immer mehr Studiendaten hin. Investoren stellen sich die Frage: Wann greift "Big Pharma" zu?
"Starker Fortschritt" und "signifikantes Interesse" - Enrollment unmittelbar vor Abschluss
Mit Edasalonexent hat Catabasis den derzeit aussichtsreichsten, steroidfreien Phase-3-DMD-Produktkandidaten für alle Erkrankten im Portfolio - und eilt mit großem Tempo in Richtung Zulassung. So mache das Screening der Patienten "starken Fortschritt" und die Rekrutierung an den weltweiten Studienzentren verlaufe "schnell". Medizinchefin Joanna Donovan kommentierte:
Das Interesse der Familien und die Begeisterung der Forscher weltweit sind groß, und die Einschreibung läuft sehr gut, da einige Länder bereits ausgelastet sind.
In den letzten neun Monaten hat Catabasis stolze 37 Forschungszentren weltweit für die laufende PolarisDMD-Studie an den Start gebracht und es fehlen nur noch drei. Somit rechnen wir mit einem offiziellen Enrollment-Abschluss im Verlaufe des kommenden Monats Juli. Ein Jahr später soll der Daten-Readout erfolgen, auf dessen Basis man Anfang 2021 den Zulassungsantrag in den USA stellen will. Wir gehen davon aus, dass Catabasis bereits vorher von der Börse verschwunden ist - per Buyout.

Auf der PPMD 2019 ist jeder namhafte DMD-Player vertreten - und jene, die es gerne wären...
Sarepta, Pfizer - oder Roche?
Über sehr gute Gründe für einen Catabasis-Buyout durch Pfizer oder Sarepta hatten wir bereits spekuliert. Hier und hier sind unsere Einschätzungen nachzulesen. Pfizer hatte im vergangenen Jahr einen Phase-2-Flop vermeldet. Gleichzeitig sank damit die Erwartung an den DMD-Wirkstoff von Roche, der zur gleichen Medikamentenklasse gehört.
Es liegt nun auf der Hand, dass die Big Pharmas im DMD-Universum auf der Suche nach einem möglichst weit fortgeschrittenen Kommerzialisierungskandidaten sind, um von Beginn an eine starke Position in einem zukunftsträchtigen Markt einzunehmen. Sarepta kommt mit seiner vor weniger als drei Jahren zugelassenen Gentherapie Exondys 51 bereits auf rund 400 Millionen Dollar Jahresumsatz - obwohl die Therapie nur bei 13% der DMD-Erkrankten angewendet wird! Exondys 51, dessen Effektivität fragwürdig ist und in Europa zunächst nicht zugelassen wurde, hat einen Listenpreis von unfassbaren 892.000 Dollar pro Jahr!
Es verdichten sich die Hinweise, dass Catabasis Edasalonexent nicht nur als potenziell exzellente Grundtherapie für alle DMD-Erkrankten und künftig auch in weiteren Indikationen wie der Becker-Muskeldystrophie vermarkten kann, sondern auch als Kombinationspräparat mit Dystrophin-orientierten Therapien, wie etwa Sareptas Exondys 51.
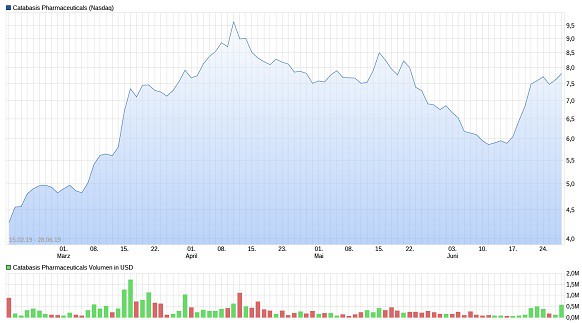
Nur noch kleinere Gewinnmitnahmen halten derzeit dagegen: Wann knallt der Kurs endgültig dahin, wo er hingehört? Quelle: ariva.de
Der Preis ist heiß - großer Vortrag heute nach Börsenschluss
Catabasis wird heute Abend um 22:30 Uhr deutscher Zeit die große Bühne der Parent Project Muscular Dystrophy dazu nutzen, einen mündlichen Vortrag über Edasalonexent zu halten. Es würde uns nicht wundern, wenn auch der Markt weitere bedeutende News serviert bekäme!
Wir sind uns sicher: Das Catabasis-Management rund um Gründerin und CEO Jil Milne würde einem Buyout zu einer Enterprise Valuation von weniger als 500 Millionen Dollar nicht zustimmen. Selbst eine Milliarde Dollar erscheint angesichts der Deal-Historie der Big Pharmas und dem lukrativen Feld der Pediatric Rare Disease alles andere als zu hoch gegriffen.
Mit einer Zulassung Edasalonexents in 2021 würde das Unternehmen außerdem einen der seltenen, veräußerbaren Priority Review Vouchers erhalten. Dieser allein sollte einen dreistelligen Millionenwert repräsentieren.
Dass dies alles nicht zu einer gegenwärtigen Marktkapitalisierung von knapp 90 Millionen Dollar und einer vollfinanzierten Zulassungsstudie passt, sollte jedem einleuchten. Es ist wie immer nur eine Frage der Zeit, bis die Wall Street den fairen Wert erkennt und einpreist (Beispiel Palatin Technologies) - oder ein Buyout den Prozess beschleunigt (Beispiel Immune Design).
Interessenkonflikt: Autor, Herausgeber, Mitarbeiter und NBC-Clubmitglieder halten selbstverständlich Aktien des besprochenen Unternehmens. Somit besteht konkret und eindeutig ein Interessenkonflikt. Autor, Herausgeber, Mitarbeiter und NBC-Clubmitglieder beabsichtigen, die Aktien – je nach Marktsituation auch kurzfristig – zu kaufen oder zu veräußern und könnten dabei von erhöhter Handelsliquidität profitieren.



